Kalorimeter: Unterschied zwischen den Versionen
Admin (Diskussion | Beiträge) (Die Seite wurde neu angelegt: Ein '''Kalorimeter''' (lat. calor = Wärme) ist eine Apparatur zur Bestimmung der Wärmeenergie, die bei einem Prozessen umgesetzt wird. Man unterscheidet Kalorimet...) |
Admin (Diskussion | Beiträge) (→Aufbau) |
||
| Zeile 2: | Zeile 2: | ||
== Aufbau == |
== Aufbau == |
||
[[Bild:Kalorimeter |
[[Bild:Kalorimeter.gif|thumb|schematischer Aufbau]]Die Abbildung zeigt die grundsätzlichen Elemente eines typischen Kalorimeters. Das zu untersuchende System ist entweder ein reiner Stoff oder ein Stoffgemisch. Elektrischer Widerstand , Rührer und Thermometer tauchen in eine Flüssigkeit, die das zu untersuchende System umschliesst. In der Regel steht das System unter Atmosphärendruck (offenes Kalorimeter), der während der Messung als konstant betrachtet wird. Die gemessenen Wärmen erhalten den Index ''p''. Sind an der chemischen Reaktion Gase beteiligt, befinden sich die Reaktanden in einem dickwandigen Stahlgefäss unter hohem Gasdruck (Bombenkalorimeter). In diesem Fall bleibt das Volumen des Systems konstant, nicht der Druck. Die gemessenen Wärmen erhalten den Index ''V''. |
||
[[Kategorie:Thermo]] |
[[Kategorie:Thermo]] |
||
Aktuelle Version vom 16. Juli 2008, 15:09 Uhr
Ein Kalorimeter (lat. calor = Wärme) ist eine Apparatur zur Bestimmung der Wärmeenergie, die bei einem Prozessen umgesetzt wird. Man unterscheidet Kalorimeter nach den Betriebsarten (adiabatisch oder isotherm) bzw. nach dem Messprinzip (Leistungskompensations- oder Wärmeleitungsprinzip). Kalorimeter für die Messung der bei einer chemischen Reaktion umgesetzten Reaktionswärme werden als Reaktionskalorimeter bezeichnet.
Aufbau
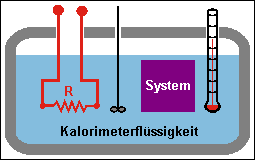
Die Abbildung zeigt die grundsätzlichen Elemente eines typischen Kalorimeters. Das zu untersuchende System ist entweder ein reiner Stoff oder ein Stoffgemisch. Elektrischer Widerstand , Rührer und Thermometer tauchen in eine Flüssigkeit, die das zu untersuchende System umschliesst. In der Regel steht das System unter Atmosphärendruck (offenes Kalorimeter), der während der Messung als konstant betrachtet wird. Die gemessenen Wärmen erhalten den Index p. Sind an der chemischen Reaktion Gase beteiligt, befinden sich die Reaktanden in einem dickwandigen Stahlgefäss unter hohem Gasdruck (Bombenkalorimeter). In diesem Fall bleibt das Volumen des Systems konstant, nicht der Druck. Die gemessenen Wärmen erhalten den Index V.