Joule-Zyklus: Unterschied zwischen den Versionen
Admin (Diskussion | Beiträge) |
Admin (Diskussion | Beiträge) |
||
| Zeile 59: | Zeile 59: | ||
</gallery> |
</gallery> |
||
== Wirkungsgrad == |
|||
Version vom 12. Mai 2008, 06:57 Uhr
Der Joule-Kreisprozess oder Brayton-Kreisprozess ist eine Idealisierung des in Gasturbinen und Strahltriebwerken ablaufenden Vorganges. Der Joule-Zyklus setzt sich aus zwei isentropen und zwei isobaren Zustandsänderungen zusammen.
Beschreibung
Im idealen Joule-Zyklus oder Joule-Kreisprozess wird das Gas isentrop kompimiert, isobar geheizt, isentrop entspannt und zum Schluss isobar gekühlt
- 1 - 2 isentrope Kompression (spezifische Entropie bleibt konstant)
- 2 - 3 isobares Heizen (Druck bleibt konstant)
- 3 - 4 isentrope Expansion (spezifische Entropie bleibt konstant)
- 4 - 1 isobares Kühlen (Druck bleibt konstant)
| Zustandsdiagramme | |
|---|---|
 |
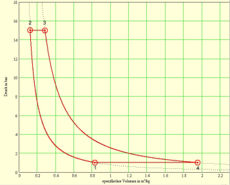 |
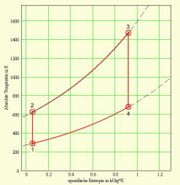
Die Fläche unter dem T-S-Diagramm entspricht der Wärme (thermisch ausgetauschte Energie) und die Fläche unter dem p-V-Diagramm der (negativen) Arbeit (mechanisch ausgetauschte Energie). Die ausgeschnittene Fläche ergibt in beiden Diagrammen die mechanisch frei gesetzte Energie. Die beiden Basisprozesse, aus denen der Joule-Zyklus zusammengesetzt wird, lassen sich thermisch, kalorisch oder entropisch beschreiben
| Prozess | thermisch | entropisch | energetisch | Bemerkung |
|---|---|---|---|---|
| isobar | [math]\displaystyle{ \frac {v}{v_0}=\frac {T}{T_0} }[/math] | [math]\displaystyle{ \Delta s=c_p ln\frac{T}{T_0} }[/math] | [math]\displaystyle{ \Delta h=c_p\Delta T }[/math] | Gesetz von Gay-Lussac |
| isentrop | [math]\displaystyle{ (\frac{v}{v_0})^{R_s}=(\frac{T_0}{T})^{c_V} }[/math] | [math]\displaystyle{ \Delta s=0 }[/math] | [math]\displaystyle{ \Delta w=c_V\Delta T }[/math] | [math]\displaystyle{ \kappa=\frac{c_p}{c_V} }[/math] |
Die mengenartigen Grössen Entropie, Volumen, Energie und Enthalpie sind klein geschrieben, weil damit spezifische Grössen (Menge pro Masse) gemeint sind. Die Wärmekapazität bei konstantem Volumen cV und bei konstantem Druck cp sowie die Gaskonstante Rs sind ebenfalls auf die Masse bezogen (spezifisch). Die thermische Beschreibung für die isentrope Zustandsänderung kann mit Hilfe des Isentropenexponentes [math]\displaystyle{ \kappa = \frac {c_p}{c_V} }[/math] umgeschrieben werden
- [math]\displaystyle{ (\frac{v}{v_0})^{\kappa -1}=\frac{T_0}{T} }[/math]
Unter Verwendung der spezifischen Gasgleichung [math]\displaystyle{ pv=R_sT }[/math] oder [math]\displaystyle{ p=\varrho R_sT }[/math] lässt sich dieser Zusammenhang in eine Form mit den Variablen p und v umwandeln
- [math]\displaystyle{ (\frac{v}{v_0})^\kappa=\frac{p_0}{p} }[/math]
Eine weitere Umformung liefert
- [math]\displaystyle{ (\frac{p}{p_0})^{\kappa -1}=(\frac{T}{T_0})^\kappa }[/math]
Simulation
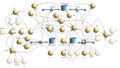
Der Joule-Zyklus kann mit Hilfe des Carnotor simuliert werden. Die nachfolgenden Bilder zeigen das Systemdiagramm des Carnotors, die Gleichungen sowie die beiden Zustandsdiagramme, das Temperatur-Entropie-Diagramm und das Druck-Volumen-Diagramm.
-
Systemdiagramm (flowchart)
-
Gleichungen
-
T-S-Diagramm
-
p-V-Diagramm