Joule-Zyklus
Der Joule-Kreisprozess oder Brayton-Kreisprozess ist eine Idealisierung des in Gasturbinen und Strahltriebwerken ablaufenden Vorganges. Der Joule-Zyklus setzt sich aus zwei isentropen und zwei isobaren Zustandsänderungen zusammen.
Beschreibung
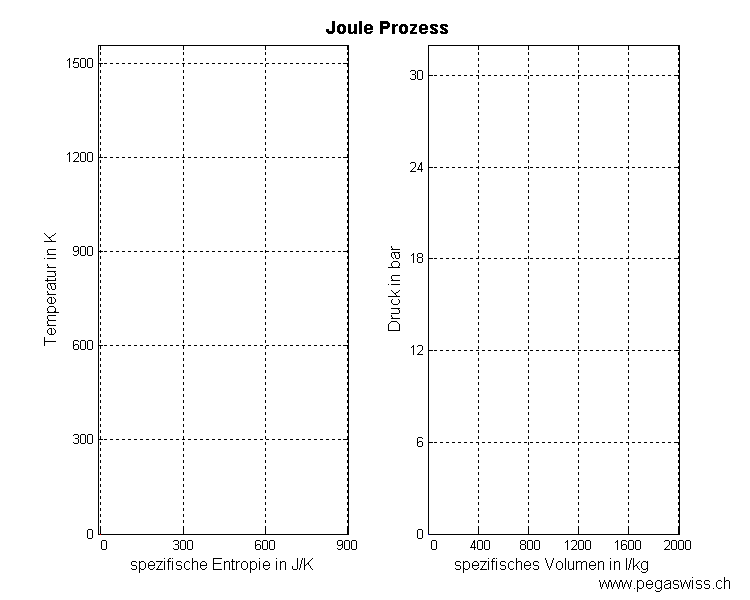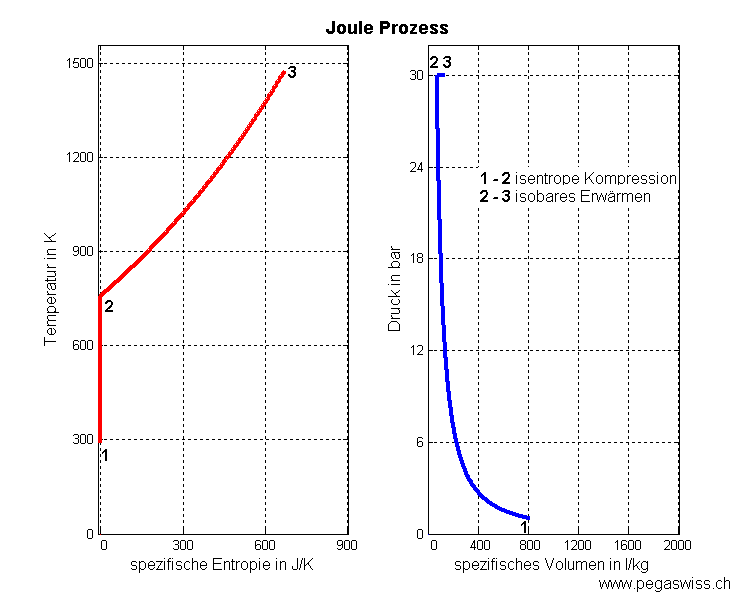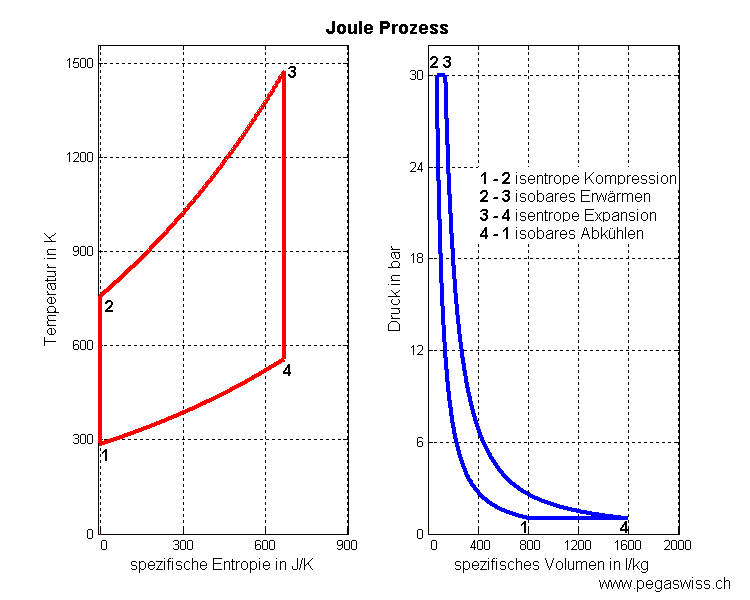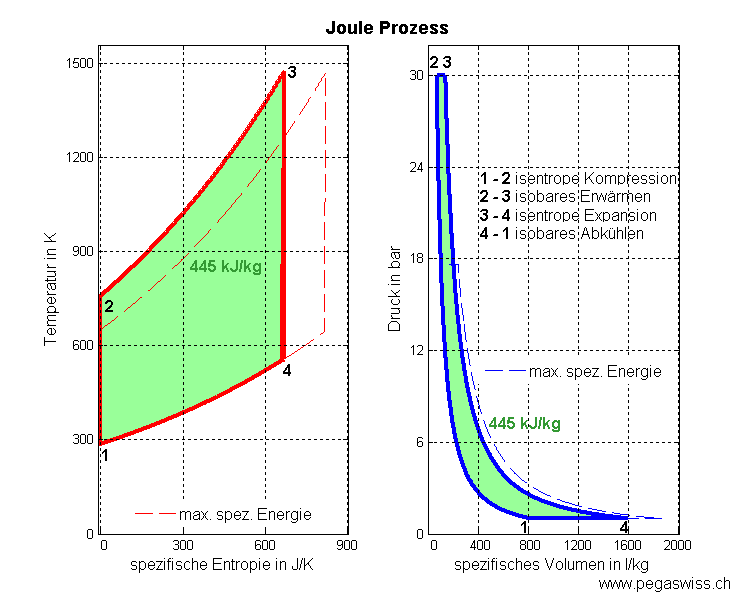
Im idealen Joule-Zyklus oder Joule-Kreisprozess wird das Gas isentrop kompimiert, isobar geheizt, isentrop entspannt und zum Schluss isobar gekühlt
- 1 - 2 isentrope Kompression (spezifische Entropie bleibt konstant)
- 2 - 3 isobares Heizen (Druck bleibt konstant)
- 3 - 4 isentrope Expansion (spezifische Entropie bleibt konstant)
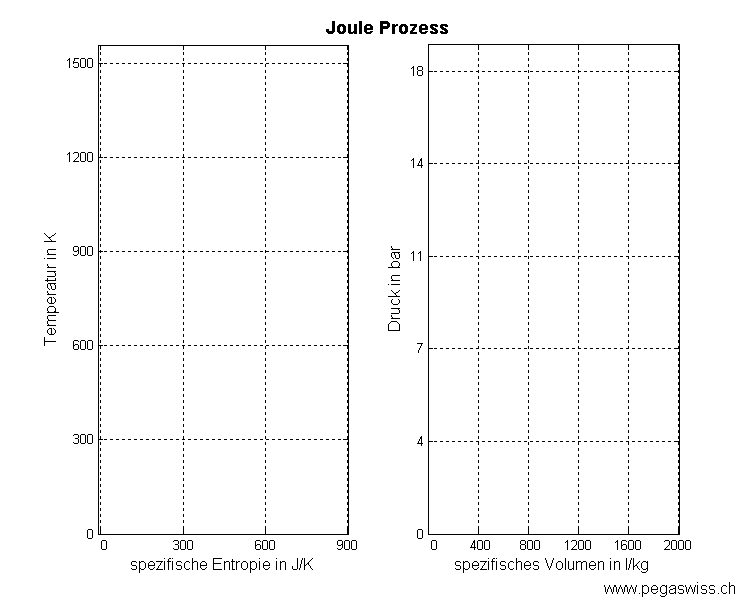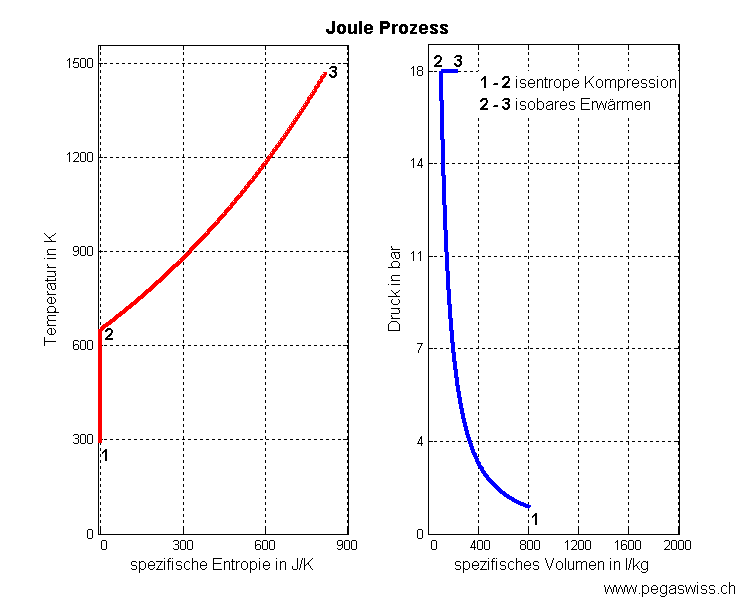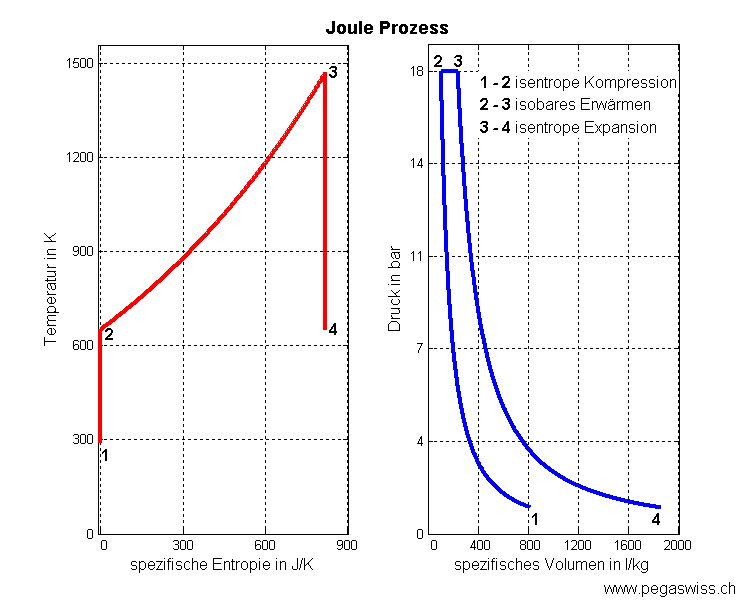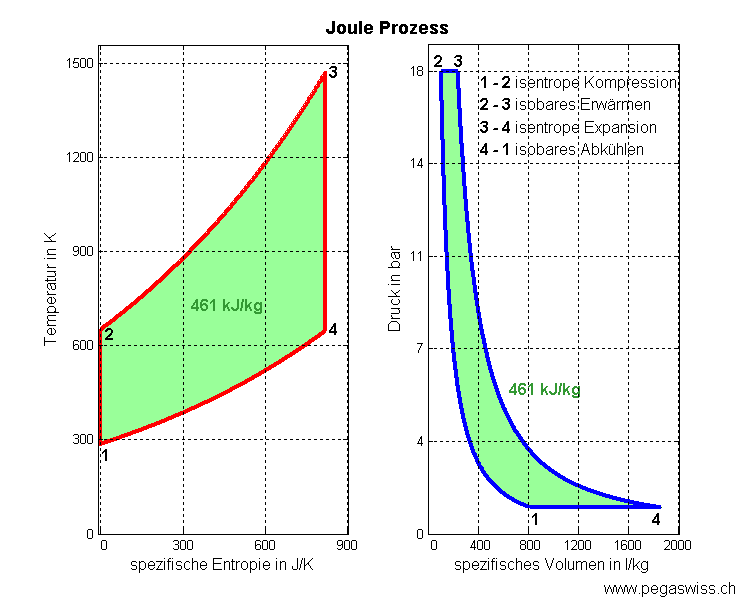
- 4 - 1 isobares Kühlen (Druck bleibt konstant)
| Zustandsdiagramme | |
|---|---|
 |
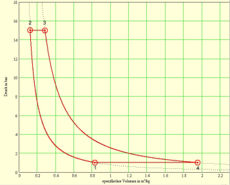 |
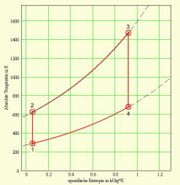
Die Fläche unter dem T-S-Diagramm entspricht der Wärme (thermisch ausgetauschte Energie) und die Fläche unter dem p-V-Diagramm der (negativen) Arbeit (mechanisch ausgetauschte Energie). Die ausgeschnittene Fläche ergibt in beiden Diagrammen die mechanisch frei gesetzte Energie. Die beiden Basisprozesse, aus denen der Joule-Zyklus zusammengesetzt wird, lassen sich thermisch, kalorisch oder entropisch beschreiben
| Prozess | thermisch | entropisch | energetisch | Bemerkung |
|---|---|---|---|---|
| isobar | [math]\displaystyle{ \frac {v}{v_0}=\frac {T}{T_0} }[/math] | [math]\displaystyle{ \Delta s=c_p ln\frac{T}{T_0} }[/math] | [math]\displaystyle{ \Delta h=c_p\Delta T }[/math] | Gesetz von Gay-Lussac |
| isentrop | [math]\displaystyle{ (\frac{v}{v_0})^{R_s}=(\frac{T_0}{T})^{c_V} }[/math] | [math]\displaystyle{ \Delta s=0 }[/math] | [math]\displaystyle{ \Delta w=c_V\Delta T }[/math] | [math]\displaystyle{ \kappa=\frac{c_p}{c_V} }[/math] |
Die mengenartigen Grössen Entropie, Volumen, Energie und Enthalpie sind klein geschrieben, weil damit spezifische Grössen (Menge pro Masse) gemeint sind. Die Wärmekapazität bei konstantem Volumen cV und bei konstantem Druck cp sowie die Gaskonstante Rs sind ebenfalls auf die Masse bezogen (spezifisch). Die thermische Beschreibung für die isentrope Zustandsänderung kann mit Hilfe des Isentropenexponentes [math]\displaystyle{ \kappa = \frac {c_p}{c_V} }[/math] umgeschrieben werden
- [math]\displaystyle{ (\frac{v}{v_0})^{\kappa -1}=\frac{T_0}{T} }[/math]
Unter Verwendung der spezifischen Gasgleichung [math]\displaystyle{ pv=R_sT }[/math] oder [math]\displaystyle{ p=\varrho R_sT }[/math] lässt sich dieser Zusammenhang in eine Form mit den Variablen p und v umwandeln
- [math]\displaystyle{ (\frac{v}{v_0})^\kappa=\frac{p_0}{p} }[/math]
Eine weitere Umformung liefert
- [math]\displaystyle{ (\frac{p}{p_0})^{\kappa -1}=(\frac{T}{T_0})^\kappa }[/math]
maximale Leistung
Oft sind Druck und Temperatur im Punkt eins gegeben (z.B. bei Gasturbinen und Strahltriebwerke). Zudem darf die Gastemperatur beim Eintritt in die Turbine (T3) einen bestimmten Wert nicht überschreiten, weil sonst die Schaufeln beschädigt würden. Damit bleibt nur noch eine Grösse, die frei gewählt werden kann (z.B. der Druck nach dem Kompressor p2).
- Komprimiert man die Luft schwach, steigt auch die Temperatur T2 nur wenig an. Das Gas muss danach stark aufgeheizt werden, bis es die maximale Turbineneintritts-Temperatur T3 erreicht hat. Im T-s-Diagramm bildet dann die vom Joule-Zyklus umrandete Fläche, die Nettoarbeit pro Kilogramm Luft, eine schmale Sichel und im p-v-Diagramm ein flaches Viereck.
- Wird die Luft so stark komprimiert, dass sie beim Austritt aus dem Kompressor schon fast die Maximaltemperatur T3 erreicht hat, kann sie danach nur noch wenig geheizt werden. Die umrandete Fläche bildet dann im T-s-Diagramm ein schmales Viereck mit zwei gebogenen, kurzen Kanten, den Isobaren. Im p-v-Diagramm wird dieser Zyklus als feine Sichel dargestellt.
Zwischen diesen beiden Prozessführungen liegt ein Optimum, bei dem die frei gesetzte Energie pro Kilogramm Gas maximal wird. Geht man von einem kontinuierlichen Gasstrom aus, ist die maximal mögliche Leistung unter den gegebenen Randbedingungen (Druck Temperatur der Umgebung sowie Maximaltemperatur) erreicht, sobald diese spezifische Energie maximal ist.
Die nutzbare Energie pro Kilogramm Luft ist gleich der thermisch zugeführten Energie (spezifische Reaktionsenthalpie) minus der thermisch abgeführten Energie (Abwärme)
- [math]\displaystyle{ w=c_p(T_3-T_2)+c_p(T_1-T_4)=c_p\left(T_3\left(1-\frac{T_4}{T_3}\right)+T_1\left(1-\frac{T_2}{T_1}\right)\right) }[/math]
Zur weiteren Analyse führen wir folgende dimensionslose Kenngrössen ein
- Druckverhältnis: [math]\displaystyle{ \pi=\frac{p_2}{p_1}=\frac{p_3}{p_4} }[/math]
- Temperaturverhältnis: [math]\displaystyle{ \tau=\frac{T_3}{T_1} }[/math]
Mit der Abkürzung [math]\displaystyle{ \frac{\kappa-1}{\kappa}=m }[/math] können die Temperaturverhältnisse bei den isentropen Prozessen wie folgt in ein Druckverhältnis umgeschrieben werden
- [math]\displaystyle{ \pi^m=\frac{T_2}{T_1}=\frac{T_3}{T_4} }[/math]
Daraus folgt für die nutzbare Energie
- [math]\displaystyle{ w=c_pT_1\left(\tau\left(1-\frac{1}{\pi^m}\right)+\left(1-\pi^m\right)\right) }[/math]
Die nutzbare Energie ist gleich Null, falls das Druckverhältnis gleich 1 oder maximal [math]\displaystyle{ \left(\pi^m=\tau\right) }[/math] ist. Um die maximale spezifische Energie zu bestimmen, leitet man die Energie nach dem Druckverhältnis ab und sucht die Nullstelle, was zu folgender Bedingung führt
- [math]\displaystyle{ \tau=\pi^{2m} }[/math] oder [math]\displaystyle{ \frac{T_3}{T_1}=\left(\frac{T_2}{T_1}\right)^2 }[/math]
Die so optimierte Temperatur nach dem Kompressor entspricht damit dem geometrischen Mittel aus Maximal- und Minimaltemperatur
- [math]\displaystyle{ T_2=\sqrt{T_1T_3} }[/math]
Die maximal nutzbare spezifische Energie ist damit gleich
- [math]\displaystyle{ w=c_pT_1\left(\pi^{2m}-2\pi^m+1\right)=c_p\left(T_3-2\sqrt{T_1T_3}+T_1\right)=c_p\left(\sqrt{T_3}-\sqrt{T_1}\right)^2 }[/math]
Wirkungsgrad
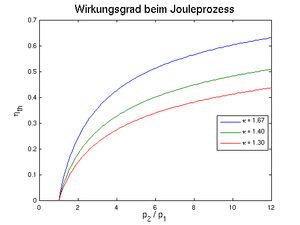
Der thermodynamische Wirkungsgrad ist als Verhältnis von Nutzenergie (frei verfügbare Energie) zu zugeführter Wärmeenergie definiert. Diese Definition liefert auch bei reversibler Prozessführung einen Wert kleiner eins. Wird die Entropie bei konstanter Temperatur aufgenommen und bei einer zweiten wieder abgegeben, ergibt sich bei einem idealen (reversiblen) Prozess der so genannte Carnot-Wirkungsgrad
- [math]\displaystyle{ \eta_C=\frac{W_{Nutz}}{W_{th,zu}}=\frac{W_{th,zu}-W_{th,ab}}{W_{th,zu}}=\frac{T_{hoch}S-T_{tief}S}{T_{hoch}S}=\frac{T_{hoch}-T_{tief}}{T_{hoch}}=1-\frac{T_{tief}}{T_{hoch}} }[/math]
Weil die Temperatur im Joule-Kreisprozess beim Heizen und Kühlen nicht konstant bleibt, kann auch im reversiblen Fall nicht die Formel des Carnot-Wirkungsgrads angewendet werden. Ausgehend von der Definition des thermodynamischen Wirkungsgrades
- [math]\displaystyle{ \eta=\frac{w}{w_{th,zu}}=\frac{c_p(T_3-T_2)-c_p(T_4-T_1))}{c_p(T_3-T_2)}=1-\frac{\left(\frac{T_4}{T_1}-1\right)T_1}{\left(\frac{T_3}{T_2}-1\right)T_2}=1-\frac{1}{\pi^m} }[/math]
Die bei der letzten Umformung gekürzten Klammerterme sind gleich gross, weil das Verhältnis von T4 zu T1 gleich T3 zu T2 ist. Dies folgt aus der Gleichsetzung der zugeführten zur abgeführten Entropie. Im idealen Joule-Zyklus hängt der Wirkungsgrad also nur vom Druckverhältnis der Kompression ab. Je höher komprimiert wird, desto grösser der Wirkungsgrad. Im Grenzfall T2 = T3 wird der Carnot-Wirkungsgrad erreicht. Nur ist dann die pro Kilogramm Luft freigesetzte Energie gleich Null. Bei der maximalen Leistung (maximal freigesetzte Energie pro Kilogramm Luft) verringert sich der Wirkungsgrad auf
- [math]\displaystyle{ \eta=1-\frac{1}{\sqrt{\tau}}=1-\sqrt{\frac{T_1}{T_3}} }[/math]
Maximale Leistung und optimaler Wirkungsgrad schliessen sich beim Joule-Prozess aus. Deshalb geht man bei Strahltriebwerken einen Kompromiss ein ein und legt den Joule Prozess zwischen maximale spezifische Energie (kleines Triebwerk) und maximalen Wirkungsgrad (beste Verwertung des Brennstoffs).
Simulation
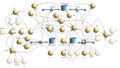
Der Joule-Zyklus kann mit Hilfe des Carnotor simuliert werden. Die nachfolgenden Bilder zeigen das Systemdiagramm des Carnotors, die Gleichungen sowie die beiden Zustandsdiagramme, das Temperatur-Entropie-Diagramm und das Druck-Volumen-Diagramm.
-
Systemdiagramm (flowchart)
-
Gleichungen
-
T-S-Diagramm
-
p-V-Diagramm