Wärme als Entropie
Wärme kann gespeichert und transportiert, aber auch erzeugt werden. Sucht man in der Physik nach einer Grösse, die auf diese Umschreibung zutrifft, stösst man auf die Entropie. Entropie ist das Fachwort aus der Physik für die Wärmemenge der Umgangssprache. Leider ist der Begriff Wärme Mitte des 19. Jahrhunderts im Zusammenhang mit dem ersten Hauptsatz der Thermodynamik anders definiert worden. Deshalb versteht man in der Physik unter Wärme die Energie, die zusammen mit der Entropie über die Systemgrenze transportiert wird.
Entropie ist eine bilanzierbare Grösse der Physik. Zudem trägt jeder leitungsartige Entropiestrom einen (thermischen) Energiestrom über die Systemgrenze, wobei die absolute Temperatur das Energiebeladungsmass darstellt. Mikroskopisch macht sich die gespeicherte Entropie in einer Vergrösserung der Zustandssumme bemerkbar. Unter der Zustandssumme versteht man die Zahl der mikroskopischen Anordnungen, die im gleichen makroskopischen Zustand (Druck, Temperatur, Volumen, Stoffmenge, chemisches Potenzial) möglich sind.
Lernziele
Sie lernen in dieser Vorlesung
- dass Entropie ein anderes Wort für Wärme im Sinne der Umgangssprache ist
- dass Entropie in J/K und Entropieströme in W/K gemessen werden
- wie die in einem thermischen Prozess freigesetzte oder aufgenommene Leistung berechnet wird
- wie gross die in einem irreversiblen Prozess erzeugte Entropie ist
- wie eine Wärmekraftmaschine oder eine Wärmepumpe im Prinzip funktioniert
Entropiespeicher
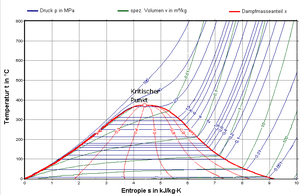
Entropie kann temperaturwirksam (manifest) oder ohne Temperaturveränderung (latent) gespeichert werden. Betrachten wir dazu ein Stück Eis, das in einem mit verschiebbaren Kolben verschlossenen Zylinder eingegossen ist. Der Kolben sorgt für einen konstanten Druck im Innern des Zylinders. Heizt man das System langsam auf, steigt die Temperatur des Eises kontinuierlich an. Bei 0°C bleibt die Temperatur trotz Wärmezufuhr über längere Zeit konstant. Dabei wandelt sich das Eis in Wasser um. Danach steigt die Temperatur wieder an, bis der Verdampfungspunkt erreicht ist. Bei der Verdampfungstemperatur, deren konkreter Wert stark vom herrschenden Druck abhängt, bleibt die Temperatur erneut stehen und das Wasser wandelt sich in Dampf (gasförmiger Zustand) um. Schlussendlich steigt die Temperatur des Dampfes wieder kontinuierlich an.
Die oben geschilderten fünf Heizphasen können in zwei verschiedene Gruppen eingeteilt werden
- manifest: Speicherung von Entropie durch Temperaturanstieg von festen, flüssigen und gasförmigen Körpern
- latent: Speicherung von Entropie durch Umwandlung von fest in flüssig oder von flüssig in gasförmig
Gasförmige (und im beschränkten Umfang auch flüssige und feste) Stoffe können Entropie manifest und latent speichern
- manifest: das Gas speichert Entropie infolge Temperaturanstieg bei konstant gehaltenem Volumen
- latent: das Gas speichert Entropie mittels Volumenvergrösserung bei konstant gehaltener Temperatur
Auf dieser doppelten Speicherfähigkeit basieren die meisten Prozesse, die in Wärmekraftmaschinen und Wärmepumpen ablaufen.
Ein Gemisch speichert mehr Entropie als die noch ungemischten Reinstoffe bei sonst gleichem Zustand (Temperatur, Druck). Mischentropie tritt auf, wenn
- sich zwei Gase (gleicher Druck, gleiche Temperatur) mischen
- Salz in Wasser gelöst wird
- Wasser in Luft verdunstet
Weil Entropie auch produziert werden kann, wird bei vielen Mischvorgängen die dazu notwendige Entropie direkt erzeugt. Beim Entmischen muss die Mischentropie, unabhängig ob sie vorher erzeugt oder zugeführt worden ist, an die Umwelt abgeführt werden.
Impuls und Drehimpuls sind lange Zeit nicht als Primärgrössen der Physik wahrgenommen worden, weil wir diese Mengen praktisch unbeschränkt der Erde entnehmen können. Mit der Entropie verhält es sich ähnlich. Erschwerend kommt hinzu, dass die Entropie in einem sich selbst überlassenen System, den unter den gegebenen Umständen maximalen Wert annehmen kann. Eine Grösse, die überall zu haben ist und sich zudem andauernd vermehrt, hat praktisch keinen Marktwert. Und dennoch wird die Zukunft unserer Zivilisation stark vom richtigen Umgang mit der Entropie abhängen.
zugeordneter Energiestrom
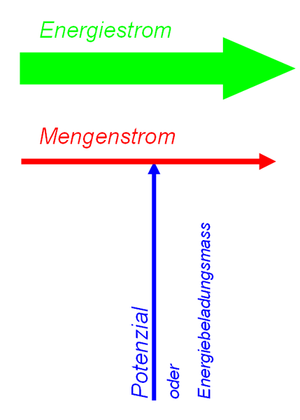
Die Energie tritt in der Thermodynamik wie in allen andern Zweigen der Physik als reine Buchhaltungsgrösse auf. Dass in der Wärmelehre einzelne Sachverhalte mit der Energie statt mit der Entropie erklärt werden, hängt mit der Verlässlichkeit der thermischen Energie bei total irreversibeln Vorgängen zusammen. Mit solchen Prozessen werden wir uns aber erst in einer späteren Vorlesung auseinander setzten. Zuerst wollen wir uns mit der Bedeutung der Entropie als Energieträger beschäftigen. In dieser Hinsicht lässt sich die Entropie ohne Einschränkung in das allgemeine Schema der Physik der dynamischen Systeme einordnen.
| Gebiet | Menge | Einheit | Potenzial | Einheit |
|---|---|---|---|---|
| Gravitation | Masse | kg | Gravitationspotenzial | J/kg |
| Hydrodynamik | Volumen | m3 | Druck | Pa |
| Elektrodynamik | elektrische Ladung | C, As | elektrisches Potenzial | J/C, V |
| Translationsmechanik | Impuls | Ns, kgm/s | Geschwindigkeit | m/s |
| Rotationsmechanik | Drehimpuls | Nms, kgm2/s | Winkelgeschwindigkeit | 1/s |
| Thermodynamik | Entropie | J/K | absolute Temperatur | K |
Dass in der historischen Entwicklung der Thermodynamik etwas schief gelaufen ist, erkennt man schon bei den Einheiten. Im Gegensatz zur Elektrodynamik, wo die Ladung in Coulomb und das Potenzial in Joule pro Coulomb gemessen wird, hat man in der Thermodynamik das Potenzial, die Temperatur, als Basiseinheit ausgewählt. Die eigentliche Primärgrösse, die Entropie, bekommt keine eigene Einheit und wird immer nur in Joule pro Kelvin angegeben.
Als Formelzeichen für die Entropie wird der Buchstabe S verwendet. Fliesst nun Wärme leitungsartig durch eine Referenzfläche der Temperatur T, kann dem Entropiestrom IS ein Energiestrom IW zugeordnet werden
- [math]\displaystyle{ I_W=T I_S }[/math]
Oft wird nur die Stärke des thermischen Energiestromes IW (gemessen in Watt) angegeben. Daraus lässt sich die Entropiestromstärke IS (gemessen in Watt pro Kelvin) problemlos berechnen, indem der Energiestrom durch die absolute Temperatur der Referenzfläche dividiert wird.
Prozessleistung
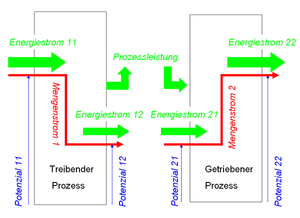
Die Vorstellung, dass ein Wärmestoff (Entropie) beim Hinunterfallen treibende Kraft (Energie) frei setzt, geht auf Sadi Carnot zurück. Weil Carnot bei seinen Überlegungen annahm, dass die Entropie unter allen Umständen erhalten bleibt und die treibende Kraft bei unsorgfältigem Umgang verschwendet wird, konnten seine Ideen nicht ohne Widerspruch in eine tragfähige Grundlage der Thermodynamik umgearbeitet werden. Hätte er damals schon bemerkt, dass die Verschwendung von treibender Kraft immer mit einer Wärmeproduktion verbunden ist, wäre die Thermodynamik damals nicht so verknorzt formuliert worden.
Geht man von einer reversiblen Prozessführung aus, also von einem Prozess, bei dem keine Entropie erzeugt wird, trifft das von Carnot gezeichnete Bild voll zu. Fliesst Entropie von einem heissen Körper zu einem kalten, setzt der Wärmestrom eine Prozessleistung frei
- [math]\displaystyle{ P=(T_1-T_2)I_S }[/math]
Diese Prozessleistung kann nutzen, wer zwischen den beiden Körpern eine Wärmekraftmaschine laufen lässt. Mit dieser Formel ordnen wir den thermischen Prozess in eine ganze Reihe von Elementarprozessen ein
- Gravitationsprozess: die Masse des Wassers fliesst von einem Stausee in einen tiefer gelegenen See
- [math]\displaystyle{ P=g(h_1-h_2)I_m }[/math]
- hydraulischer Prozess: das Volumen des Hydrauliköls strömt von einem Hochdruck- in einen Niederdruckbehälter
- [math]\displaystyle{ P=(p_1-p_2)I_V }[/math]
- elektrischer Prozess: elektrische Ladung fliesst aus einem geladenen Kondensator in einen ungeladenen
- [math]\displaystyle{ P=(U_1-U_2)I }[/math]
- translatorischer Prozess: Impuls fliesst von einem schnellen Fahrzeug in ein langsameres über
- [math]\displaystyle{ P=(v_{x_1}-v_{x_2})F_x }[/math]
- rotatorischer Prozess: Drehimpuls strömt aus einem schnell drehenden Schwungrad in ein langsameres
- [math]\displaystyle{ P=(\omega_{x_1}-\omega_{x_2})M_x }[/math]
- thermischer Prozess: Entropie fliesst aus einem heissen in ein kaltes System
- [math]\displaystyle{ P=(T_1-T_2)I_S }[/math]
In dieser Zusammenstellung fehlt noch ein letzter Prozess, mit dem wir uns aber in diesem Kurs nicht beschäftigen werden. Stoffmenge, die aus einem Gebiet mit grossem in ein Gebiet mit kleinem chemischen Potenzial strömt, setzt eine Prozessleistung frei, die ebenfalls gleich dem Produkt aus Potenzialdifferenz mal Stromstärke ist.
Entropieproduktion
In jedem Reibungsprozess wird Entropie produziert. Weil Entropie erzeugt, aber nicht vernichtet werden kann, liegt immer dann ein Reibungsprozess vor, wenn sich der Vorgang in der Zeit nicht umkehren lässt. In der Zeit umkehrbare Prozesse nennt man reversibel, nicht umkehrbare irreversibel. Die Entropieproduktion sorgt dafür, dass eine Zeitreise in die Vergangenheit nicht möglich ist.
reversible Vorgänge
Streng genommen sind exakt reversible Vorgänge nicht möglich, weil schon bei der Beobachtung (Messvorgang) eine minimale Entropiemenge produziert wird. Folgende Modelle verhalten sich im Prinzip reversibel, erzeugen also keine Entropie
- schiefer Wurf (nur eigentliche Bewegung ohne Abwurf oder Aufschlag)
- nicht gedämpfter Ein- oder Zweimassenschwinger
- physisches Pendel
- Bewegung der Himmelskörper
irreversible Prozesse
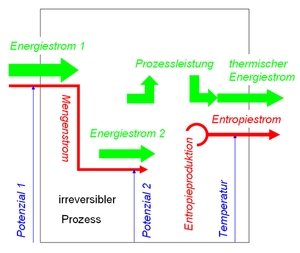
Ein irreversibler Prozess liegt vor, wenn die im Prozess freigesetzte Leistung von keinem weiteren Prozess aufgenommen wird. Dann muss die Prozessleistung auf die zu produzierende Entropie umgeladen werden. Geht man davon aus, dass die produzierte Entropie das Gebiet ihrer Entstehung (Temperatur T) in Form eines Wärmestromes verlässt, ist im stationären Zustand der weg fliessende Entropiestrom betragsmässig gleich der Produktionsrate
- [math]\displaystyle{ I_S+\Pi_S=0 }[/math]
Weil dann der dem weg fliessenden Entropiestrom zugeordnete Energiestrom gleich der Prozessleistung ist, gilt für die Produktionsrate der Entropie
- [math]\displaystyle{ \Pi_S=\frac{P_{diss}}{T} }[/math]
Der Index diss soll darauf hinweisen, dass die Leistung dissipiert wird, dass die Energie für weitere Prozesse nicht mehr zur Verfügung steht.
Beispiele:
| Prozess | Leistung |
|---|---|
| Wasserfall | [math]\displaystyle{ P_{diss}=g(h_1-h_2)I_m }[/math] |
| langes Rohr | [math]\displaystyle{ P_{diss}=(p_1-p_2)I_V }[/math] |
| Widerstand | [math]\displaystyle{ P_{diss}=UI=RI^2=\frac{U^2}{R} }[/math] |
| Knautschzone | [math]\displaystyle{ P_{diss}=(v_1-v_2)F }[/math] |
| Rutschkupplung | [math]\displaystyle{ P_{diss}=(\omega_1-\omega_2)M }[/math] |
| Wärmeleitung | [math]\displaystyle{ P_{diss}=(T_1-T_2)I_S }[/math] |
Die Wärmeleitung nimmt eine gewisse Sonderstellung ein, weil im Primärprozess die gleiche Grösse "hinunter fällt" wie im Sekundärprozess produziert wird. Zur Berechnung der Entropieproduktionsrate muss die tiefere Temperatur eingesetzt werden, weil die Wärme auf diesem Niveau weg fliesst.
Wärmepumpen
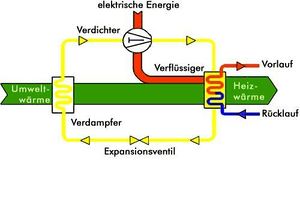
Eine Wärmepumpe fördert Wärme (Entropie) von einem System tiefer Temperatur (kaltes Wärmebad) in ein System hoher Temperatur (heisses Wärmebad). Eine Wärmepumpe kann zum Heizen oder Kühlen eines Gebäudes oder eines Raumes eingesetzt werden. Beim Heizen befindet sich der Nutzer auf der warmen Seite (Wärmepumpe gibt Entropie ab), beim Kühlen auf der kalten (Wärmepumpe zieht Entropie ab).
Beispiel 1: Eine Wärmepumpe soll einen thermischen Energiestrom von 4 kW an 47°C warmes Wasser abgeben. Wie viel Prozessleistung muss sie mindestens aufnehmen, wenn sie Wärme aus dem 7°C warmen Grundwasser wegpumpt?
Lösung: In einem ersten Schritt berechnet man die Stromstärke der abzugebenden Entropie
- [math]\displaystyle{ I_S=\frac{I_W}{T_2}=\frac{4000 W}{320 K} }[/math] = 12.5 W/K
Die minimale Prozessleistung (reversible Prozessführung) ist dann gleich
- [math]\displaystyle{ P=(T_2-T_1)I_S=40K*12.5W/K }[/math] = 500 W
Würde man die Entropie direkt mit Hilfe eines total irreversiblen Prozesses erzeugen (z.B. mit einer Elektroheizung), wäre die Prozessleistung gleich 4 kW.
Beispiel 2: Eine Kühltruhe (Innentemperatur -23°C) benötigt in 24 Stunden 1.2kWh elektrische Energie. Wie viel Wärmeenergie würde sie in dieser Zeit bei idealer Prozessführung über den Wärmetauscher an der Rückwand (Temperatur 47°C) abgeben?
Lösung: In 24 Stunden würde eine ideale Wärmepumpe die folgende Entropiemenge fördern
- [math]\displaystyle{ S=\frac{W}{T_2-T_1}=\frac{4.32 MJ}{70 K} }[/math] = 61.7 kJ/K
Diese Entropie trägt die folgende Energie
- [math]\displaystyle{ W_{therm}=ST_2=61.7kJ/K*320K }[/math] = 19.7 MJ = 5.5 kWh
Ein Teil dieser Energie und auch der Entropie fliesst in diesen 24 Stunden im Kreis herum.
Wärmekraftmaschinen
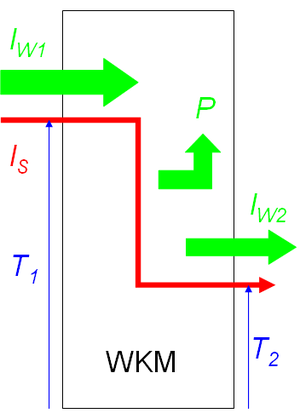
Entropie, die aus einem System hoher Temperatur in ein kälteres überfliesst, besitzt ein Arbeitsvermögen, das von Wärmekraftmaschinen genutzt wird. Die dabei freigesetzte Prozessleistung berechnet sich nach der allgemeinen Formel
- [math]\displaystyle{ P=(T_1-T_2)I_S }[/math]
Zur Illustration dieser Beziehung untersuchen wir die Wärmeströme bezüglich des Sekundärkreises eines Druckwasserreaktors. Im Verdampfer wird das Wasser unter hohem Druck und entsprechend hoher Temperatur verdampft. Der so erzeugt Dampf strömt danach durch eine Turbine und gibt dort Energie an den durch die Welle fliessenden Drehimpuls ab. Dabei kühlt sich der Dampf ab, d.h. manifeste Entropie geht in latente über. Neben der Temperatur verringert sich dabei auch der Druck. Im Kondensator gibt der Dampf so lange Entropie an den Kühlkreislauf ab, bis er ganz zu Wasser geworden ist. Danach bringt ein Pumpsystem das Wasser wieder auf den im Verdampfer herrschenden, hohen Druck.
Zum KKW Brokdorf findet man folgende Daten:
Primärkreis
| Betriebsdruck | 157 bar (15,7 MPa) |
| Kühlmitteltemperatur beim Eintritt in Reaktor | 291.3 °C |
| Kühlmitteltemperatur beim Austritt aus Reaktor | 326.1 °C. |
| Kühlmittelstrom | 67680 t/h |
| Reaktorleistung | 3765 MW |
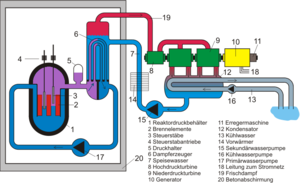
Sekundärkreis
| Temperatur der Vorwärmanlage | 218°C |
| Sattdampferzeugung | 2,061 t/s (285°/ 66 bar) |
| Generatorleistung | 1395 MW |
| Generatorspannung | 27 kV |
Kühlkreis
| Kühlmittelstrom | 208008 t/h |
| max. Wassertemperatur | 33°C |
Geht man davon aus, dass die gesamte Reaktorleistung dem verdampfenden Wasser zugeführt wird, nimmt dieses bei 285°C den folgenden Entropiestrom auf
- [math]\displaystyle{ I_{S1}=\frac{I_{W1}}{T_1}=\frac{3.765 GW}{558 K} }[/math] = 6.75 MW/K
Zieht man die Generatorleistung von 1395 MW von der Reaktorleistung ab, erhält man eine Kühlleistung von 2.37 GW. Diese Energie wird bei 33°C von einem Entropiestrom weggetragen, dessen Stärke wie folgt berechnet werden kann
- [math]\displaystyle{ I_{S2}=\frac{I_{W2}}{T_2}=\frac{2.37 GW}{306 K} }[/math] = 7.75 MW/K
Die Entropieproduktionsrate im Sekundärkreislauf beträgt demnach 1 MW/K oder knapp 15% des zufliessenden Entropiestromes. Will man mehr mechanische Leistung gewinnen, muss die Entropie auf höherem Temperaturniveau zugeführt werden.
Dampfmaschinen funktionieren nach einem ähnlichen Prinzip, nur wird dort die Entropie zusammen mit dem Dampf abgeführt. Bei Verbrennungsmotoren wird die Entropie direkt im Arbeitszylinder erzeugt und dann zusammen mit den kalten Gasen an die Umgebung abgegeben. Gasturbinen und Strahltriebwerke sind Verbrennungsmotoren mit kontinuierlichem Durchsatz.
Kontrollfragen
- Eine Kochherdplatte gibt bei einer mittleren Oberflächentemperatur von 327°C einen Energiestrom von 1800 W ab. Wie stark ist der zugehörige Entropiestrom?
- Die Heizschlangen der oben erwähnten Kochherdplatte weisen eine Temperatur von 387°C auf. Wie gross ist die Entropieproduktionsrate in diesen Heizschlangen?
- Das Kühlsystem entzieht einer Kühltruhe bei -23°C einen Energiestrom von 500 W. Wie stark ist der zugehörige Entropiestrom?
- Das Kühlsystem gibt die Wärme bei 37°C an einen Wassertank ab. Welche (elektrische) Leistung muss dieses Kühlsystem mindestens aufnehmen?
- Eine Wärmepumpe fördert die Wärme aus der -3°C warmen Umgebung in das 37°C warme Wasser der Bodenheizung. Welche (elektrische) Leistung muss die Wärmepumpe mindestens aufnehmen, damit sie einen thermischen Energiestrom (Heizleistung) von 6 kW abgeben kann?
Antworten zu den Kontrollfragen
- Der die Energie tragende Entropiestrom ist gleich Energiestrom durch absolute Temperatur, also gleich 3 W/K.
- Die Entropieproduktionsrate ist gleich dissipierte Prozessleistung durch dort herrschende Temperatur, also gleich 2.727 W/K.
- Der Entropiestrom ist gleich Energiestrom durch absolute Temperatur, also gleich 2 W/K.
- Die Pumpleistung ist gleich Entropiestrom mal Temperaturdifferenz, also gleich 120 W.
- Die Wärmepumpe gibt einen Entropiestrom der Stärke 6 KW : 310 K = 19.35 W/K an das warme Wasser ab. Um diesen Entropiestrom um 40°C "hinauf" zu pumpen, benötigt die Wärmepumpe eine minimale Leistung von 774 W.
Materialien
- Skript Seiten 1 und 2
- Physik - Ein systemdynamischer Zugang für die Sekundarstufe II Seiten 116 - 125
- Videoaufzeichnung 2009
- Videoaufzeichnung 2010
- Kurzfassung auf Youtube